您现在的位置是: 首页 > 招生信息 招生信息
2015高考化学全国卷1答案,2015化学高考真题
tamoadmin 2024-05-20 人已围观
简介1.一道高考化学题B详细解答如下:设烧瓶体积为1L。①干燥纯净的氨气c=n/V=1/22.4除以1L溶液=1/22.4 mol/L②含一半空气的氯化氢n(HCl)=0.5L除以22.4L=1/44.8 mol溶液的体积也只有一半即0.5L(其余的为空气,水不能进入)所以浓度也=1/22.4 mol/L③NO2和O2的混合气体[V(NO2):V(O2)=4:7]即NO2有4/11L,氧气有7/1
1.一道高考化学题
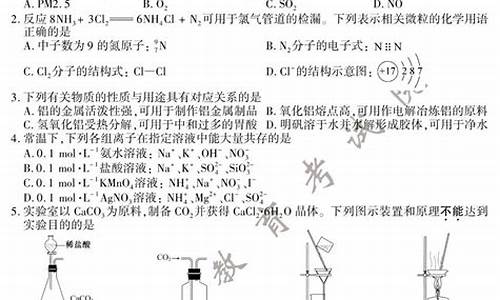
B
详细解答如下:设烧瓶体积为1L。
①干燥纯净的氨气c=n/V=1/22.4除以1L溶液=1/22.4 mol/L
②含一半空气的氯化氢n(HCl)=0.5L除以22.4L=1/44.8 mol溶液的体积也只有一半即0.5L(其余的为空气,水不能进入)所以浓度也=1/22.4 mol/L
③NO2和O2的混合气体[V(NO2):V(O2)=4:7]即NO2有4/11L,氧气有7/11L
发生反应:4NO2+O2+2H2O=4HNO3
则生成的硝酸为1/61.6 mol 溶液的体积为5/11L
硝酸的浓度=1/28 mol/L
所以三者的浓度之比为
1/22.4 mol/L:1/22.4 mol/L:1/28 mol/L = 5:5:4
选B
一道高考化学题
分析:
A.容器Ⅰ中从正反应开始到达平衡,容器Ⅱ中从逆反应开始到达,平衡建立的途径不相同;
B.容器Ⅲ中相当于在容器Ⅰ中平衡的基础上再加入1mol CO和1mol H2O,反应向正反应进行,故容器Ⅲ中到达平衡时温度更高,该反应正反应是放热反应,温度越高平衡常数越小;
C.容器Ⅱ中所到达的平衡状态,相当于在容器Ⅰ中平衡的基础上降低温度,平衡向正反应移动;
D.温度相同时,容器Ⅰ中CO 的转化率与容器Ⅱ中CO2的转化率之和等于1,容器Ⅱ中所到达的平衡状态,相当于在容器Ⅰ中平衡的基础上降低温度,平衡向正反应移动.
解答:
解:
A.容器Ⅰ中从正反应开始到达平衡,容器Ⅱ中从逆反应开始到达,平衡建立的途径不相同,无法比较反应速率,故A错误;
B.容器Ⅲ中相当于在容器Ⅰ中平衡的基础上再加入1mol CO和1mol H2O,反应向正反应进行,故容器Ⅲ中到达平衡时温度更高,该反应正反应是放热反应,温度越高平衡常数越小,故B错误;
C.容器Ⅱ中所到达的平衡状态,相当于在容器Ⅰ中平衡的基础上降低温度,平衡向正反应移动,故容器Ⅰ中CO 的物质的量比容器Ⅱ中的多,故C正确;
D.温度相同时,容器I中CO 的转化率与容器Ⅱ中CO2的转化率之和等于1,容器Ⅱ中所到达的平衡状态,相当于在容器Ⅰ中平衡的基础上降低温度,平衡向正反应移动,二氧化碳的转化率比两容器相同温度时容器Ⅱ中CO2的转化率低,故容器Ⅰ中CO 的转化率与容器Ⅱ中CO2的转化率之和小于1,故D正确.
故选CD.
C选项涉及到一个用氮气吹洗溶液的问题,因为氮气是惰性气体,所以向溶液中通入N2可以将溶解的NO2吹离溶液。在利用分光光度法检验亚硝酸胺的实验中就有利用通入N2吹出NO的操作,电化学实验中所配的溶液以及医学上的某些药液中也要通入氮气以除氧。在本题中如果加入N2后溶液变色,就说明溶液是因为溶有NO2而显绿色的。所以C项可以~不过这ms不是咱高中内容了呢...
A选项和C的目的相同,也是除去溶解的NO2。如果加热后颜色变回成正常的绿色则说明溶有NO2,即乙是对的,否则甲对。
B你应该懂吧~因为加了水溶液颜色变浅,无法分辨是那种原因。
而D,它的意思是另取一份蓝色的饱和硝酸铜溶液,向其中通入NO2,要是溶液同样变为绿色,那么乙的猜想就是对的。
但愿这些能对你有所帮助^ - ^









